「私の論文」
この論文は、立案から実験は湯川眞希さんが行ったので、私の論文とは言いがたい。私のしたのは投稿原稿の完成と、雑誌の編集者との駆け引きであった。しかし、最も記憶が鮮明なので取り上げる事にした。
葉緑体のNAD(P)H脱水素酵素(NDH)は25種以上の成分からなり、タバコ葉緑体ゲノムはその内の11種の遺伝子を持っている(ndhAからK)。ndhCとndhKのコード領域(シストロン)は一部が重複している。すなわち、ndhCの停止暗号UAGの4ヌクレオチド(GUCU)前方にndhKの開始暗号AUGがある。従って両者のシストロンは別の読み枠となっている。大腸菌、そのファージや動物RNAウィルスにはこのような例がある。通常、前方のシストロンを読んだリボソームが、次の後方のシストロンも読む(共役翻訳)。この場合、多くのリボソームは停止暗号の所でmRNAから外れてしまい、一部が少し前に戻って、後方のシストロンを翻訳するので、その翻訳量は極めて低い。葉緑体の場合、ndhCとndhKの産物NdhCとNdhKは同じ量合成されないとNDHはできないと考えられる。葉緑体ゲノムにはndhCとndhKは各1個しかないので、NdhCとNdhKはこの重複mRNAからしか合成できない。
葉緑体ゲノムがコードするタンパク質の大部分は複合体の構成成分で、量比は決っていることが多い。例えば、リボソームの成分は等モルずつである。葉緑体の翻訳の研究は、核遺伝子の変異体を使ったり、葉緑体形質転換で調べられている。翻訳に関与する因子の探索や、翻訳の活性化の因子を同定するなどの成果を上げている。しかし、翻訳速度あるいは翻訳量を測ったりするには向いていない。1990年代に廣瀬哲郎君が、タバコの単離葉緑体からin vitro(無細胞)翻訳系の開発に成功した。その後、改良に改良を重ね、極めて高活性の系が出来上がった。
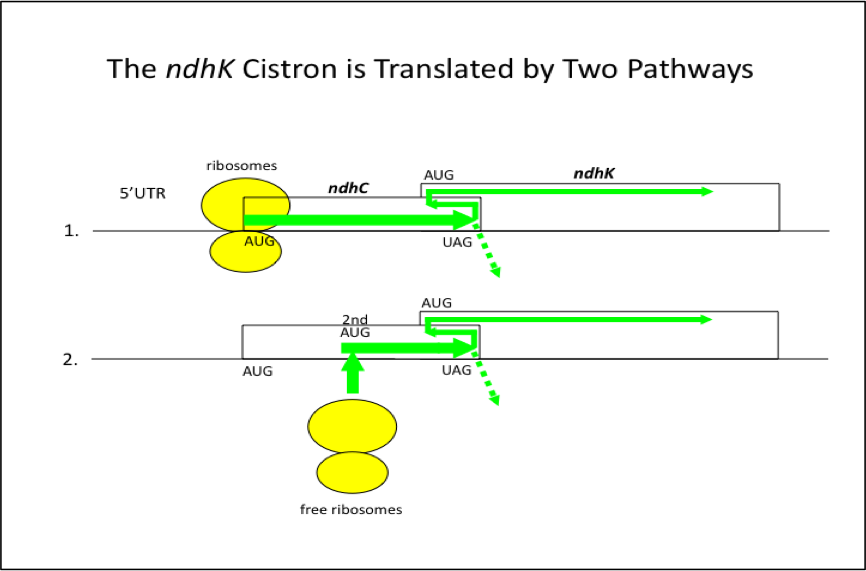
図に示すようなndhC-ndhK mRNA鋳型をin vitro系で翻訳すると、予想に反してほぼ等量合成された。そこで5’非翻訳領域(5’UTR)とそれに続くndhCの開始コドンを除いたmRNAをつくってin vitro翻訳すると、驚いた事にかなりの量のNdhKが合成された。
共役翻訳の常識からすれば、後方のシストロンは5’UTRに入ったリボソームが前方のシストロンを読み終わり、ついで後方のシストロンを読むはずである。リボソームの入口である5’UTRを除いてしまっているから、当然後方のシストロンは全く読めないことになる。湯川さんは、おかしい、おかしい、私の実験の腕が鈍ったかと云っていた。彼女の技術が確かなことは私が一番良く知っていたので、未知の新しい翻訳経路があるだろうと考え論文化した(Proc. Natl. Acad. Sci. 2008)。
次に、この新しい経路に取り組むことにした。まず考えられることは、前方のndhC配列が5’UTRの役目をして後方のndhKを読むと云うものである。しかし、前述の5’UTRを除いたmRNAで、ndhCの終止暗号UAGを変異させると、ndhKの翻訳は全く起きないという結果を既に得ていた。これはndhCのUAGをリボソームが認識する、言い換えれば前方のndhCの読み枠を識別することになる。ndhCシストロン内には、開始暗号AUG以外に、同じ読み枠に3個のAUGが存在することが分かった。リボソームは、これら3個または1個のAUGから入るかもしれない。AUGに1個ずつ変異を入れたmRNAで調べると、第2番目(ndhCのほぼ中央)のAUG(2nd AUG)を壊すと翻訳が起きないことがわかった。そこで、リボソームは2nd AUGに入り、読み枠に従って進み停止暗号まで行き着く。リボソームの多くはここでmRNAから外れてしまうが、一部は4ヌクレオチド戻って、別枠のndhKシストロンのAUGを識別して、ここから翻訳を始めると云うモデルが一番単純である。では、どうしてリボソームは進むのだろうか。ひとつは、核由来のmRNAのようにリボソームはスキャンしてUAGまでたどり着くものである。これだと余分の素材やエネルギーを使わずにすむので考えやすい。しかし、スキャニングを証明するのは極めて難しい。
次は、2nd AUGから翻訳しながらリボソームが進むものである。これなら翻訳産物の57アミノ酸のペプチドが出来ることになる。何とも無駄な話である。しかし、これだと何とか証明ができそうである。葉緑体プロテオームの論文を調べたが記載は見当たらなかった。NDH自体チラコイドタンパク質の0.2%以下とのことで無理もないことである。そこで実際に実験してみることにした。in vitro系で合成するので極めて微量にしかできなく、染色では無理である。そこでRIか蛍光標識でラベルすることにした。幸い蛍光標識したLys-tRNAとfMet-tRNAが市販されている。この試薬はバッチによりばらつきがあり、バックが高過ぎで使用できないものもあった。通常、反応液は20μl以下であるが、これを数倍にすることも試した。しかし、葉緑体抽出液からより高活性のS30画分が調製できるようになったので、標準は20μlとした。57アミノ酸のペプチド(6.5 kDa)の検出は困難を極めた。普通ならここで投げ出してしまうところである。湯川さんは辛抱強く何度も繰り返し、2〜3年後にかすかなバンドを検出した。これでは読者に納得してもらうには充分とは云えない。そこで、翻訳活性の強いファージT7 gene10の5’UTRを2nd AUGの前に付けた。これにより、やっときれいな6.5 kDaのバンドが得られた。そこで、第2の経路として2nd AUGからフリーのリボソームが入り、ndhCの後半を翻訳しながら進み、この一部はまたndhKを翻訳し、第1の経路と合わせてNdhCとNdhKがほぼ等量合成されるというモデルを提唱することにした。第2の経路は57アミノ酸よりなるペプチドを合成するという代償を払うことになる。
論文にまとめ投稿すると、in vivoで証明せよとのコメントが返ってきた。現時点の技術レベルでは最初から無理だと解っていたが、湯川さんは一応葉緑体内に57 kDaペプチドが有るかどうかを調べた。結果はだめであった。私は長い長い説明を編集者に書き送った。その結果、マイナーな字句修正だけで、ほとんど元の原稿のままで受理された。この編集者をすごく尊敬している。幸いこの成果は平成25年3月19日の中日新聞に「ママ研究員 — いきいき」と題して大きく掲載された。
我々のin vitro系を使った原稿には、いつもin vivoではどうか、in vivoで証明せよとコメントが来る。ひどい場合は、30分も反応させればmRNAは壊れてしまうというコメントもあった。これは、単なる葉緑体抽出液とin vitro系のS30画分と混同している。in vitro系というものは、年という単位で、成功するかどうかも分からずに、失敗に失敗を重ねてやっと開発するものである。翻訳の基本的な分子機構は、すべて、主として大腸菌のin vitro系を使って解明された。例えば、全遺伝暗号の解読がそうである。これらの成果がすべてin vivoで証明されているわけでなく、信じているだけである。これは転写でも同じで、まずRNAポリメラーゼの精製から始まった。スプライシングも、イントロンの発見から5年後にHeLa細胞のin vitro系が開発されて、やっと機構の解析が始まった。遺伝子発現の基本機構はまずin vitro解析からである。植物の研究者は、時間と労力のかかる解析をすっ飛ばし、大腸菌、酵母や動物細胞で得られた成果をそのまま植物に当てはめて、検証もせずにいる。この辺は反省してみる必要がありそうだ。